El Ministerio de Salud ha lanzado una campaña para evitar la multiplicación de casos de dengue. Son pasos sencillos y fáciles de seguir. Higiene en ciertos lugares de la casa Se recomienda lavar los bordes de las pilas y se sugiere que con un mascón (u otro utensilio) se laven barriles una vez por semana. Eliminar los depósitos que estén vacíos No acumular depósitos vacíos (botellas, latas, corcholatas, huacales, cascarones de huevo, estopas de coco) dentro y fuera de la casa. Desechar neumáticos que ya no sirven Salud exhorta a que las personas destruyan las llantas inservibles, o llenarlas con tierra para que no puedan acumular agua. Tomar medidas para prevenir enfermedad En las pilas y todos los depósitos con agua (como los barriles) se pide colocar bolsitas matalarvas, que pueden adquirirse gratis. Acudir al médico ante emergencia Si tiene fiebre, dolor de cabeza, no siente apetito y tiene dolor abdominal, el Ministerio de Salud recomienda consultar al m...
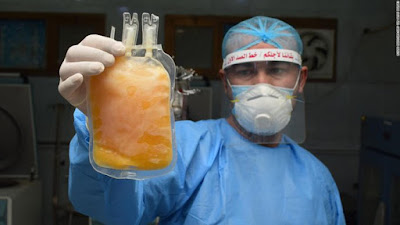 Los datos hasta el momento indican cierta eficacia en su uso temprano en la enfermedad, aunque faltan ensayos clínicos y no parece un tratamiento estrella.
Los datos hasta el momento indican cierta eficacia en su uso temprano en la enfermedad, aunque faltan ensayos clínicos y no parece un tratamiento estrella.
Comentarios
Publicar un comentario